Cannabis als Medizin ist weltweit im Vormarsch. Um eine Vorstellung zu erhalten welches Potenzial hier noch brach liegt und welche Folgen die kommende Normalisierung von Cannabis als Medizin in Deutschland hat lohnt ein Blick über den Atlantik. Genauer gesagt kann man in Kanada sehen wie es bei uns in einigen Jahren aussehen könnte. Dort ist – im Gegensatz zu den USA – Cannabis als Medizin bundesweit legal. Firmen bauen lizenziert und völlig legal an. Selbst einige Krankenversicherungen übernehmen die Kosten. Die Dynamik in der Cannabis als Medizin Branche ist enorm.
Genaue Statistiken zu Cannabis als Medizin
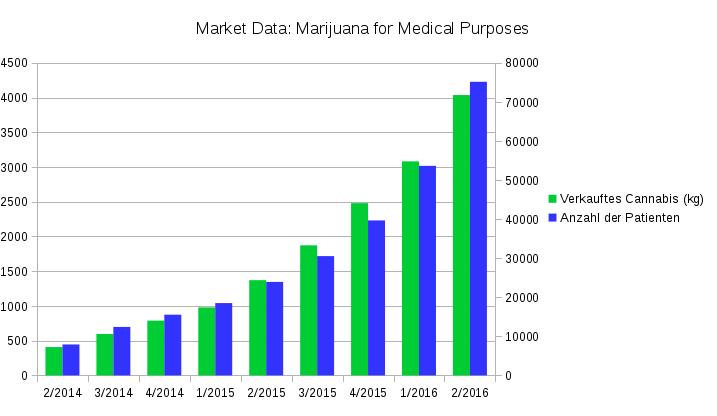
Health Canada veröffentlicht regelmäßig die Zahl der Patienten und wieviel Cannabis angebaut, gelagert und verkauft wurde. Das deutsche BfArM könnte sich hier ein Beispiel nehmen, die Zahlen für Deutschland mussten immer wieder erst extra erfragt werden. Die Daten von Health Canada umfassen derzeit den Zeitraum 2/2014 bis 2/2016. Die Mengenangaben beziehen sich immer nur auf ein Quartal.
Innerhalb der letzten zwei Jahre hat sich die Menge Cannabisblüten, die an Patienten verkauft wurden um den Faktor 10 erhöht. Mitte 2014 wurden 408 kg im Quartal bzw. hochgerechnet 1,6 Tonnen vertrieben. Im Quartal 2/2016 lag die Menge bereits bei 4037 kg. Rechnet man den Wert dieses Quartals hoch ergibt sich zusammen mit dem Wert für 1/2016 eine Gesamtmenge von 15 Tonnen für das Jahr 2016.
Die Steigerung pro Quartal lag hier bei 30-40% und das seit nunmehr 2 Jahren. Welche andere Branche (die mit realen Gütern handelt) kann hier noch mithalten? Geht man davon aus dass sich dieser Trend fortsetzen wird, könnten es für 2016 sogar 20 Tonnen Cannabisbüten werden.
Steigende Produktion und volle Lager
Die Branche darf und kann über dem Bedarf produziert. Die Produktionsmenge pro Quartal stieg von einer Tonne 2014 auf fünf Tonnen. Aktuell lagern ca. 12 Tonnen Cannabisblüten bei den Herstellern in Kanada. Diese Menge ist genug um den Bedarf bis zum Ende des Jahres abzudecken. Für die kommende Legalisierung von Cannabis als Genußmittel in Kanada ist die Branche damit vorbereitet.
Wieviel Cannabis in Zukunft nach Deutschland und andere Länder exportiert wird, wird sich zeigen. Der Preis von 15-25 € pro Gramm für Cannabis der Firma Bedrocan in Deutschland ist ein Ergebnis der rechtlichen Rahmenbedingungen. In Kanada kann die gleiche Firma Patienten allerdings schon für 3,40 € pro Gramm versorgen. Für neue Firmen, die sich auf den Anbau von Cannabis als Medizin in Deutschland bewerben wird der Import aus Kanada eine harte Konkurrenz werden.
Zusätzlich: Cannabisöl
Zurück zu den Zahlen von Health Canada: Mitte 2015 wurde die Möglichkeit geschaffen auch Cannabisöl herstellen und verkaufen zu dürfen. Jedes Gramm Öl entspricht einer bestimmten Menge Cannabis, der Umrechnungsfaktor schwankt von Produkt zu Produkt. Näherungsweise kann man rechnen 6 ml Cannabisöl = 1 g Cannabis = 6 g Cannabisöl.
1/2016 wurden 584 kg Cannabisöl angegeben. Dies entspricht etwa weiteren 3,5 Tonnen Canabisblüten im Quartal. 2/2016 waren es bereits 1,5 t Öl entspricht 6 t Blüten. Die bereits erwähnten Wachtstumsraten für die Cannabisblüten sind trotz des Booms beim Öl nicht eingebrochen. Hochgerechnet auf 2016 kommen zu den 15 bzw. 20 Tonnen Blüten noch einmal 30 Tonnen Blüten-Äquivalent in Form von Öl, welche an Patienten vertrieben werden.
Werte zu Patienten und Vergleich mit Deutschland
Die Menge Cannabis welche ein Patient im Durchschnitt pro Tag genehmigt bekommen hat lag 2014 bei 4 Gramm und inzwischen bei 2,7 Gramm. Abgerufen wurden ziemlich konstant 1 Gramm – was vermutlich wie bei uns primär eine Kostenfrage ist, wenn auch auf einem anderen Level.
Die Zahl der Patienten entwickelte sich parallel zur Menge verkauftes Cannabis. Mitte 2014 waren es 7914 Personen und der aktuellste Wert für Mitte 2016 beläuft sich auf 75166 Patienten. Der Anteil der Patienten an der Bevölkerung liegt bei etwas über 0,2%. In Deutschland sind es 0,001% der Einwohner, die eine Ausnahmegenehmigung besitzen.
In erster Näherung kann man absoluten Werte auf Deutschland übertragen. Die Einwohnerzahl liegt bei uns um den Faktor 2,3 höher. Damit müsste es in Deutschland bald – bei kanadischen Verhältnissen – 175.000 Patienten geben.
Prognose: Der Boom geht weiter
Es darf aber nicht vergessen werden dass in Kanada noch immer keine Sättigung absehbar ist und die Zahlen weiterhin steigen werden. Ausgehend von Werten aus andern Ländern könnte es in Kanada noch bis zu zwei Jahre weiter boomen und die Zahl der Patienten die Grenze von 1% der Bevölkerung überschreiten.




